Nuevo Esquema de Vacunación VCN20
Vacuna contra el neumococo
El Streptococcus pneumoniae (neumococo) es una bacteria que se encuentra de manera habitual en la mucosa nasal o faríngea (garganta) de los seres humanos. Esto hace que quienes portan la bacteria puedan transmitirla a otras personas al toser o estornudar.
El neumococo puede producir enfermedades leves (como otitis y sinusitis) y graves invasivas (como neumonía, meningitis, sepsis y artritis).
En el caso de neumonía, pueden ser fiebre, tos y dolor en tórax o pecho.
En el caso de meningitis, pueden ser fiebre, vómitos, irritabilidad y cefalea. La meningitis puede dejar secuelas auditivas y neurológicas.
Vacunación en niños
Durante el período de transición y coexistencia de VCN13 y VCN20 se priorizará el uso de la vacuna VCN20 en niños que presenten mayor riesgo de enfermedad neumocócica invasiva (ENI). Los niños sanos que inicien esquemas o hayan iniciado su vacunación con VCN13 deberán completarlo con VCN13 mientras haya disponibilidad de esta vacuna en el sector público. Cuando la misma no esté disponible, iniciarán o completarán esquema con VCN-20. Es importante remarcar que los lactantes y niños que hayan comenzado la inmunización con otra vacuna antineumocócica conjugada pueden completar la inmunización pasando a VCN20 en cualquier momento del cronograma. Los esquemas de vacunación del Calendario Nacional se continuarán recuperando en niños sanos hasta los 5 años de edad, como se encuentra contemplado actualmente. Para recupero de esquemas atrasados, se seguirán los mismos lineamientos pautados con VCN13.
Más información : Vacuna contra neumococo. Transición a la vacuna contra 20 serotipos en el Calendario Nacional de Vacunación Lineamientos técnicos y manual de vacunación.
Vacunación en Personas de 5 a 64 años
El esquema de vacunación es de 1 (una) dosis de VCN20 en pacientes con:
A. inmunocompromiso (inmunodeficiencias congénitas o adquiridas, infección por VIH, insuficiencia renal crónica, síndrome nefrótico, leucemia, linfoma y enfermedad de Hodgkin, enfermedades neoplásicas, inmunodepresión farmacológica, trasplante de órgano sólido, mieloma múltiple, asplenia funcional o anatómica, anemia de células falciformes), implante coclear y fístula de LCR.
B. Sin inmunocompromiso y con cardiopatía crónica, enfermedad pulmonar crónica, diabetes miellitus, alcoholismo, enfermedad hepática crónica, tabaquismo.
Se requerirá el esquema completo es de 4 dosis en el caso de:
C. Pacientes con Trasplante de células hematopoyéticas
El mismo será de:
- 3 dosis de VCN20 con un intervalo interdosis de 4 semanas, comenzando la vacunación entre los 3 y 6 meses post trasplante.
- Una cuarta dosis o refuerzo de VCN20 a partir de los 6 meses de la tercera dosis o 12 meses del trasplante (lo que ocurra más tarde).
Personas de 65 años y más. No se requiere orden médica. Se recomienda aprovechar la oportunidad para recibir vacuna antigripal y contra la COVID-19.
El esquema de vacunación es de 1 (una) dosis de VCN20. *
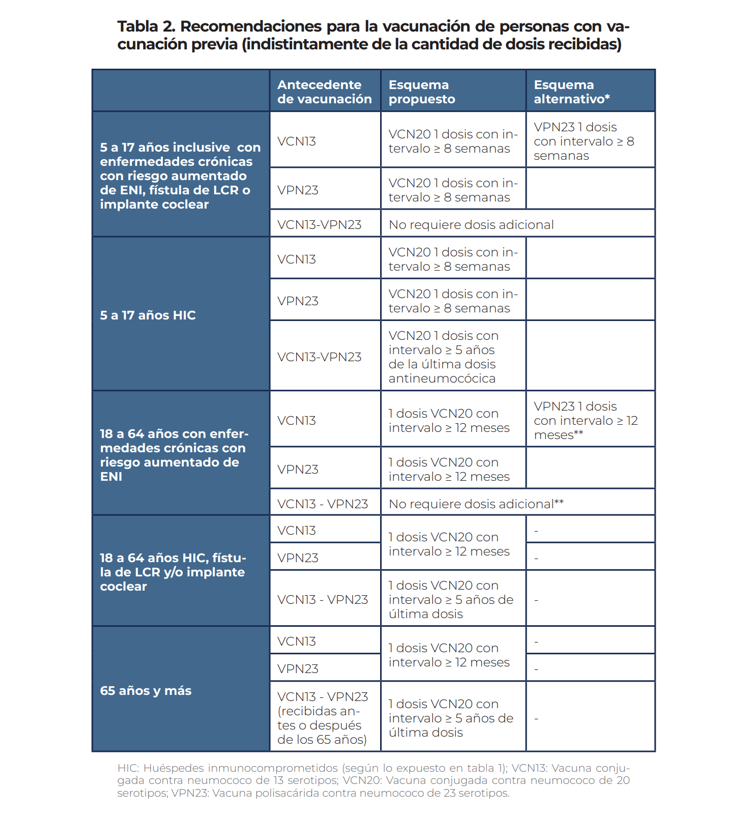
*Para las personas con antecedentes de vacunación antineumocócica previa, se debe evaluar la continuidad de esquema, según la dosis y vacuna recibida previamente, como también la edad y antecedentes médicos. Ver Tabla 2 de los lineamientos técnicos de VCN20.
Las personas con enfermedades crónicas con riesgo aumentado de enfermedad neumocócica invasiva que se aplicaron VCN13 previamente, pueden recibir como esquema alternativo la vacuna VPN23 (vacuna antineumocócica polisacárida 23 valente) si estuviera disponible. Se recomienda idealmente continuar esquema con VCN20 en personas con inmunocompromiso y mayores de 65 años.
A fin de promover la vacunación en personas con factores de riesgo se puede presentar orden médica o cualquier documentación que certifique la existencia de enfermedades preexistentes.
CONDICIONES PARA LA ELABORACIÓN, EN FARMACIAS, DE REPELENTES DE USO EXTERNO EN HUMANOS
La Dirección de Jurisdicción Farmacia (DJF), dependiente del Ministerio de Salud de la Provincia de Córdoba informa a los establecimientos categorizados como farmacias oficinales comunitarias y farmacias en establecimientos asistenciales, y que por resolución de la Dirección de Jurisdicción Farmacia -en el caso de farmacias oficinales comunitarias- tengan autorizada la elaboración de Productos Sanitarios Oficinales (PSO) según resoluciones del Ministerio de Salud de la Provincia de Córdoba 1326/2010 y su modificatoria 379/2015, en la categoría Higiene y cosmética, que quieran elaborar productos repelentes de insectos, deberán ajustarse, como indica la mencionada norma, a Io establecido en la Ley de Farmacias de la Provincia de Córdoba, a contenidos generales de las Disposiciones ANMAT referidas a Buenas Prácticas de Elaboración o Control de medicamentos, medicamentos fitoterápicos, productos para higiene y cosmética, antisépticos y desinfectantes, domisanitarios; y demás PSO de elaboración autorizada y a toda norma vigente.
Seguir leyendo: Repelentes (condiciones para su elaboración en farmacias)
LINEAMIENTOS TÉCNICOS Y MANUAL DE VACUNACIÓN: VACUNA TETRAVALENTE CONTRA EL DENGUE
El dengue se considera un problema de salud pública emergente de interés internacional ya que se ha reconocido en las últimas décadas la tendencia incremental en la magnitud de este evento y su rápida expansión geográfica hacia nuevos territorios.
A continuación pueden descargar información sobre la enfermedad y todos los aspectos que conciernen a la vacuna tetravalente existente en nuestro país.
 VACUNA TETRAVALENTE CONTRA EL DENGUE
VACUNA TETRAVALENTE CONTRA EL DENGUE
IFAs cuya condición cambiaron a Venta Libre
IFAs cuya condición cambiaron a Venta Libre
En el marco de la revisión de especialidades medicinales, instruido por Resolución MS N° 284/24, la ANMAT definió incluir el grupo terapéutico de los "prazoles" como venta libre.
De este modo, en cumplimiento de citada norma, dio inicio a la revisión de la condición de venta de especialidades medicinales. Atento lo establecido por la Disposición 3228/2024, la revisión comenzó por el grupo terapéutico perteneciente a la familia de los principios activos denominados “prazoles”, incluidos en su Anexo: OMEPRAZOL, LANSOPRAZOL, PANTOPRAZOL y ESOMEPRAZOL.
Actualmente se realizó una revisión que definió, nuevas IFAs incluidas como venta libre (delimitando concentraciones y formas farmacéuticas):
Por disposición ANMAT N° 7449/24: RETINOL / RETINALDEHIDO (VITAMINA A PALMITATO) + ALANTOINA +TOCOFEROL (VITAMINA E), RETINOL / RETINALDEHIDO (VITAMINA A PALMITATO) + ÁCIDO BÓRICO + ÓXIDO DE ZINC, AMORLFINA y ACICLOVIR.
La lista puede ser consultada ingresando en:
https://www.boletinoficial.gov.ar/detalleAviso/primera/312455/20240819
Desde el siguiente link también se puede acceder a cada una de ellas y las actualizaciones de cada IFAs en particular: https://ifasventalibre.anmat.gob.ar/ifas
https://www.boletinoficial.gov.ar/detalleAviso/primera/312455/20240819
Alerta OMS sobre OZEMPIC
La OMS ha alertado sobre tres lotes falsificados de OZEMPIC® (semaglutida) detectados en el Brasil (en octubre de 2023), el Reino Unido de Gran Bretaña e Irlanda del Norte (en octubre de 2023) y los Estados Unidos de América (en diciembre de 2023).
En los siguientes documentos encuentran información específica y cómo proceder para efectuar la denuncia correspondiente.
![]() Alerta n.° 2_2024 sobre productos médicos
Alerta n.° 2_2024 sobre productos médicos
PROTOCOLO DE MANEJO DE CASOS DE COVID-19
A continuación pueden acceder al protocolo de manejo de casos de Covid-19 elaborado por el Ministerio de Salud de la Provincia de Córdoba.
Uso inapropiado de semaglutida para el control del peso: ¿es una solución mágica?
Información actualizada sobre vacunas contra el Dengue
En la Argentina el Dengue es una enfermedad epidémica, con aparición especialmente durante los meses de mayor temperatura (noviembre a mayo) en estrecha relación con la ocurrencia de brotes en los países limítrofes.
Según datos publicados en el último Boletín Epidemiológico Nacional, hasta el 15 de abril, se notificaron en el país 56.324 casos de dengue, de los cuales 51.634 adquirieron la infección en la Argentina.
Al momento, la circulación de este virus se ha identificado en 15 jurisdicciones correspondientes a cuatro regiones: Región Centro (Buenos Aires; Ciudad Autónoma de Buenos Aires; Córdoba; Entre Ríos; Santa Fe); región Cuyo: San Luis; región NEA (Corrientes; Formosa; Chaco) y región NOA (Catamarca; Jujuy; La Rioja; Salta; Santiago del Estero y Tucumán).
Los casos acumulados registrados hasta el momento en la presente temporada están por encima de lo registrado para la misma semana en los años previos (60% más que en 2016 y 70% más que en 2020 para la misma semana).
A nivel mundial existen dos vacunas licenciadas actualmente: CYD-TDV (Dengvaxia, del laboratorio Sanofi Pasteur) y TAK-003 (Qdenga, del laboratorio Takeda) ambas son vacunas vivas atenuadas tetravalentes.
Ingresá al siguiente enlace para más información:
VACUNAS DENGUE - INFORMACIÓN OFICIAL - ARGENTINA - ( VACUNA-DENGUE )
La ANMAT aprobó el uso de la vacuna del laboratorio Takeda contra el dengue
Manual del vacunador de Pfizer Bivariante (vacunación contra COVID-19)
En enero de 2023, Argentina, incorpora la vacuna COMIRNATY BIVARIANTE, Original/Omicron BA.4-5 como dosis de refuerzo en personas de 12 años o más.
A continuación presentamos el Manual del Vacunador Vacuna COMIRNATY BIVARIANTE, Original/Omicron BA.4-5 (Vacuna COVID-19 ARNm, Pfizer-BioNTech) elaborado por el Ministerio de Salud de la Nación Argentina.
 Manual del Vacunador Pfizer Bivariante
Manual del Vacunador Pfizer Bivariante
Información Fiebre Amarilla
Con el inicio de la temporada turística, el Ministerio de Salud brinda las siguientes recomendaciones para la fiebre amarilla.
La enfermedad es de origen viral y se transmite por la picadura de ciertas especies de mosquitos. Los niños, niñas, personas mayores y aquellas que poseen factores de riesgo pueden presentar graves cuadros de la enfermedad.
La fiebre amarilla no tiene tratamiento específico, pero puede prevenirse eficazmente con la vacunación. Los síntomas de la enfermedad se presentan de forma brusca con mucha fiebre, escalofríos y dolor de cabeza. Además, pueden aparecer dolores musculares, náuseas y vómitos. Hay formas que cursan con síntomas leves e inespecíficos. Muchas veces, las formas graves causan hemorragias, insuficiencia hepática y falla orgánica múltiple.
Para conocer qué es, cómo se transmite, cómo prevenirla, la vacuna y dónde vacunarse, ingresar en: https://www.argentina.gob.ar/salud/fiebreamarilla
Es importante la consulta médica al menos 4 semanas antes del viaje para que un profesional defina la indicación o no de la vacunación.
Vacunas
La vacuna está indicada solo para quienes viven o viajen a zonas de riesgo. En Argentina, estas áreas se encuentran en las provincias de Misiones, Corrientes y Formosa, así como en ciertos departamentos de Chaco, Salta y Jujuy.
Algunos países certificado internacional de vacuna de la FA como requisito para ingresar a su territorio, antes de viajar es necesario consultar el listado de la OMS o comunicarse con el consulado o embajada del país de destino. Los requisitos de ingreso frente a la fiebre amarilla también pueden averiguarse por medio de la línea aérea a través de la cual se realizará el viaje.
En viajeros/as, la vacuna se recomienda a partir de los 2 años de edad hasta los 59 años inclusive, y debe ser aplicada al menos 10 días previos al viaje para que las personas se encuentren debidamente protegidas. Si una persona posee contraindicación para vacunarse, puede tramitar el certificado de exención en los mismos vacunatorios, así como también requerir un duplicado si ha extraviado el carné. Es importante destacar que si ya se recibió la vacuna alguna vez, no es necesario volver a aplicársela.
En Capital, la vacuna para fiebre amarilla está disponible en:
- Hospital Misericordia: Se debe solicitar turno previo al correo electrónicoinfecto.viajes.hmisericordia@gmail.com
- Hospital Pediátrico: Se solicita turno a través del 0800-555-4141, opción 1.
- Hospital San Roque Viejo: Se solicita turno a través de CiDi. Para ello, se deberá ingresar al siguiente enlace https://turnero.cba.gov.ar/turnos. Allí deberá seleccionar “Reservar turno on-line”, luego “Conozco el trámite”, escribir en el buscador “Fiebre amarilla” y elegir “Viejo Hospital San Roque” para ver la información de turnos disponibles.
En el interior, es necesario acudir al vacunatorio más cercano a su localidad, manifestar su necesidad de recibir la vacuna contra la fiebre amarilla y coordinar con el equipo de salud local el día, lugar y horario en que se aplicará dicha dosis.
Para consultar todos los vacunatorios de la Provincia de Córdoba, ingresar en: https://www.argentina.gob.ar/salud/fiebreamarilla/que-es
Documento de Posición CFC frente a la problemática de la Resistencia a los Antibióticos
En el año 2018 ya dejamos asentada la posición del Colegio de Farmacéuticos de Córdoba frente a lo que consideramos uno de los problemas de salud pública más graves y preocupantes de todo el mundo: la resistencia a los antibióticos.
A continuación, encontrarán el documento de posición elaborado por CFC en relación al uso de antibióticos al que adhirieron otras instituciones tales como: Sociedad Argentina de Pediatría – Filial Córdoba, Colegio Odontológico de la Provincia de Córdoba, Asociación Argentina de Microbiología (AAM) y Fundación Presac.
 Posición CFC - Resistencia Bacteriana
Posición CFC - Resistencia Bacteriana
Nuevo Servicio Farmacéutico Remunerado de Toma de Presión Arterial - SIAFAR
Ha sido habilitado en SIAFAR el módulo de HIPERTENSIÓN para registrar la toma de presión arterial y obtener así una remuneración por este servicio farmacéutico brindado.
Esta posibilidad está disponible para FARMACIAS COLFACOR quienes deberán seguir los pasos indicados en el siguiente instructivo para efectuar la carga de las tomas de presión arterial.
 INSTRUCTIVO CARGA EN SIAFAR - MÓDULO HIPERTENSIÓN
INSTRUCTIVO CARGA EN SIAFAR - MÓDULO HIPERTENSIÓN
Recordamos que para el paciente el servicio seguirá siendo gratuito, pero ahora la farmacia podrá cobrar su honorario en base a las tomas registradas en dicho sistema.
Protocolo para la Vigilancia Integrada SARS-CoV-2, Influenza y Otros Virus Respiratorios (OVR)
La identificación y caracterización de los virus respiratorios, así como el estudio de su frecuencia y distribución, permite direccionar las acciones de promoción, prevención y control, fortaleciendo la capacidad de respuesta de los servicios de atención de salud.
 Vigilancia Integrada Infecciones
Vigilancia Integrada Infecciones
Manual del vacunador. Vacuna Comirnaty de Pfizer-BioNTech pediátrica
Manual del vacunador. Vacuna Comirnaty de Pfizer-BioNTech pediátrica de 5 a 11 años.
Dada la posibilidad actual de contar en Argentina con la vacuna de Comirnaty pediátrica, aprobada para su uso en niños y niñas de 5 a 11 años, se utilizará esta vacuna para iniciar esquemas primarios en este grupo etario así como dosis adicional en pacientes inmunocomprometidos que hayan recibido esquema primario con Pfizer (esquemas homólogos), de acuerdo a lo que establecido por el Ministerio de Salud de la Nación, en función de las recomendaciones de la Comisión Nacional de Inmunizaciones (CoNaIn) y en consenso con el Consejo Federal de Salud (COFESA).
Vacuna antigripal 2022
Cepas recomendadas para la Vacuna antigripal 2022 según OMS
La Organización Mundial de la Salud recomienda las siguientes cepas para la formulación de vacunas contra la gripe en el hemisferio sur, para la temporada invernal 2022:
VACUNA CUADRIVALENTE O TETRAVALENTE
Vacuna producida en huevo
- un virus similar a A/Victoria/2570/2019 (H1N1)pdm09;
- un virus similar a A/Darwin/9/2021 (H3N2);
- un virus similar a B/Austria/1359417/2021 (linaje B/Victoria); y
- un virus similar a B/Phuket/3073/2013 (linaje B/Yamagata).
Vacunas recombinante y producida en cultivo celular
- un virus similar a A/Wisconsin/588/2019 (H1N1)pdm09;
- un virus similar a A/Darwin/6/2021 (H3N2);
- un virus similar a B/Austria/1359417/2021 (linaje B/Victoria); y
- un virus similar a B/Phuket/3073/2013 (linaje B/Yamagata).
VACUNA TRIVALENTE
Vacuna producida en huevo
- un virus similar a A/Victoria/2570/2019 (H1N1)pdm09;
- un virus similar a A/Darwin/9/2021 (H3N2); y
- un virus similar a B/Austria/1359417/2021 (linaje B/Victoria).
Vacunas recombinante y producida en cultivo celular
- un virus similar a A/Wisconsin/588/2019 (H1N1)pdm09;
- un virus similar a A/Darwin/6/2021 (H3N2); y
- un virus similar a B/Austria/1359417/2021 (linaje B/Victoria).
Información extraída de: Organización Mundial de la Salud (OMS). Composición recomendada de vacunas contra el virus de la influenza para usar en la temporada de influenza del hemisferio sur 2022. Disponible en:
Lineamientos Técnicos para Vacunación contra la Covid-19
Resumen de recomendaciones vigentes para la Campaña Nacional de Vacunación contra la COVID-19.
PREVENCIÓN DE EXPOSICIONES POR ACCIDENTES CON OBJETOS PUNZOCORTANTES
Nuestro rol como agentes sanitarios nos expone a diversos riesgos. En el presente documento, encontrarán información para la prevención de accidentes con objetos punzocortantes.
 PREVENCIÓN DE EXPOSICIONES POR ACCIDENTES CON OBJETOS PUNZOCORTANTES
PREVENCIÓN DE EXPOSICIONES POR ACCIDENTES CON OBJETOS PUNZOCORTANTES
Dispensa y Registro de los resultados del Autotest COVID-19
Estimados colegas en adjunto se envía información importante en relación al Servicio Profesional Farmacéutico de Dispensa y Registro de los resultados del Autotest COVID-19 .
 Instructivo SIAFAR AUTOTEST Version 2
Instructivo SIAFAR AUTOTEST Version 2
Información para pacientes: Test de Antígenos para Autodiagnóstico de Covid- 19
En el adjunto, se comparte información sobre dudas frecuentes que pueden ser planteadas por el paciente en relación a los Auto test COVID-19. Se podrá bajar dicha información, imprimir y entregar al momento de la dispensa.
Información importante para farmacias dispensadoras de Auto Test COVID-19
Estimado colega compartimos la información enviada desde COFA en relación a los Auto Test COVID-19.y la próxima puesta en marcha del proceso de dispensa en farmacias de dicho test, que seguramente dará inicio en los próximos días.
En el caso del Dossier Profesional se trata de la última versión actualizada el 19/1, y en el caso del Instructivo SIAFAR es la primera versión base para las operaciones, que seguramente será actualizado a medida que se vayan asociando nuevas funcionalidades para optimizar y facilitar la tarea de las farmacias.
Nuevo protocolo para contactos estrechos en personal estratégico priorizado. 17 de enero de 2022
 Personal estratégico priorizado
Personal estratégico priorizado
Protocolo manejo de casos de COVID-19 y sus contactos estrechos Provincia de Córdoba - 17 de enero de 2022
NUEVAS RECOMENDACIONES SOBRE EL INTERVALO DE DOSIS DE REFUERZO DE VACUNACIÓN CONTRA COVID-19
 RECOMENDACIÓN SOBRE EL INTERVALO DE DOSIS DE REFUERZO DE VACUNACIÓN CONTRA COVID-19
RECOMENDACIÓN SOBRE EL INTERVALO DE DOSIS DE REFUERZO DE VACUNACIÓN CONTRA COVID-19
ACTUALIZACIÓN PROTOCOLO COVID-19 en la Provincia de Córdoba
Protocolo adaptado del Ministerio de Salud de la Nación
 Protocolo adaptado del Ministerio de Salud de la Nación
Protocolo adaptado del Ministerio de Salud de la Nación
ACTUALIZACION DE VIGILANCIA COVID-19 en la Provincia de Córdoba
 Protocolo adaptado del Ministerio de Salud de la Nación
Protocolo adaptado del Ministerio de Salud de la Nación
Dosis adicional al esquema primario y dosis de refuerzo (booster)
 Dosis adicional al esquema primario y dosis de refuerzo (booster)
Dosis adicional al esquema primario y dosis de refuerzo (booster)
Administración de dosis adicional al esquema primario de vacunación contra COVID-19 (Argentina)
Fuente: Ministerio de Salud de la Nación, DiCEI (Dirección de Control de Enfermedades Inmunoprevenibles) | Memorándum. 26 de octubre de 2021.
La recomendación sobre aplicación de una dosis adicional en dos grupos de población definidos:
1. Personas con inmunocompromiso que hayan recibido un esquema primario con cualquier vacuna contra la COVID-19.
2. Personas de 50 años o mayores que hayan recibido un esquema primario de vacuna a virus inactivado [Sinopharm]
Autorizaciones de vacunas contra el SARS-CoV-2 en Argentina
- Vacuna SPIKEVAX (ARNm-1273), Laboratorio Moderna TX Inc. Resolución 2711/2021 Ministerio de Salud de la Nación | Fecha de autorización: 5 de octubre de 2021.
- VACUNA CONTRA COVID-19 Ad26.COV2-S (recombinante), nombre comercial COVID-19 VACCINE JANSSEN | Fecha de registro: 01 de octubre de 2021.
http://cime.fcq.unc.edu.ar/autorizaciones-de-vacunas-contra-el-sars-cov-2-en-argentina/
Noticia del Ministerio de Salud: vacunación pediátrica contra la COVID-19 (Argentina)
- En una reunión con Salud, las sociedades científicas coincidieron sobre la importancia de la vacunación pediátrica contra la COVID-19 | Publicado el miércoles 06 de octubre de 2021.
COADMINISTRACIÓN DE VACUNAS CONTRA COVID-19 CON OTRAS VACUNAS SEPTIEMBRE 2021
La evidencia disponible y recomendaciones publicadas en otros países, ha elaborado la recomendación sobre la coadministración de vacunas a partir de la cual el Ministerio de Salud define:
La posibilidad de coadministrar las vacunas contra COVID-19 junto con cualquier otra vacuna del CNV, pudiéndose administrar el mismo día o en días diferentes, sin requerir intervalo entre las dosis.
Recomendación sobre esquemas heterólogos de vacunación contra COVID-19
 Recomendación sobre esquemas heterólogos de vacunación contra COVID-19
Recomendación sobre esquemas heterólogos de vacunación contra COVID-19
VACUNACIÓN COVID EN EMBARAZADAS
Esta información forma parte del curso gratuito "Actualización en Vacunas: Covid- 19, Neumocócica y Antigripal 2021" y que se ofrece al día 24 de julio de 2021. Recordamos que en el actual contexto epidemiológico esta información puede modificarse.
 VACUNACIÓN COVID EN EMBARAZADAS
VACUNACIÓN COVID EN EMBARAZADAS
COMBINACION DE TRATAMIENTOS PARA PERSONAS INTERNADAS CON COVID 11 de Junio de 2021
La presente recomendación es dinámica y está sujeta a modificaciones en relación a la aparición de nuevas comunicaciones sobre resultados de ensayos terapéuticos
 COMBINACION DE TRATAMIENTOS PARA PERSONAS INTERNADAS CON COVID 11 de Junio de 2021
COMBINACION DE TRATAMIENTOS PARA PERSONAS INTERNADAS CON COVID 11 de Junio de 2021
Nuevo criterio para definición de caso: se incorpora Rinitis/congestión nasal
Más información en el siguiente link de acceso :
https://www.argentina.gob.ar/salud/coronavirus/definicion-de-caso
Campaña vacunación antigripal: preguntas frecuentes
 Campaña vacunación antigripal: preguntas frecuentes
Campaña vacunación antigripal: preguntas frecuentes
GUIA VACUNACIÓN ANTIGRIPAL 2021
 GUIA VACUNACIÓN ANTIGRIPAL 2021
GUIA VACUNACIÓN ANTIGRIPAL 2021
Información vacunación COVID y coadministración Vacuna antigripal y neumocóccica
 Información vacunación COVID y coadministración Vacuna antigripal y neumocóccica
Información vacunación COVID y coadministración Vacuna antigripal y neumocóccica
Protocolo de Atención de personas con COVID
 Protocolo de Atención de personas con COVID
Protocolo de Atención de personas con COVID
Información sobre Vacunación Covid-19
Fuente Dirección de Control de Enfermedades Inmunoprevenibles (DiCEI), Ministerio de Salud de la Nación |Campaña Nacional de Vacunación contra la COVID-19 | 28 de febrero 2021
La vacuna de SINOPHARM, vacuna SARS-CoV-2 (células vero) inactivada, es producida por el laboratorio del Instituto de Productos Biológicos de Beijing, de la República Popular de China. Es una vacuna monovalente compuesta por antígenos del virus SARS-CoV-2 inactivado
Se incluye el Anexo I en el cual se presentan las características de las tres vacunas presentes en Argentina para su aplicación contra COVID-19.
https://drive.google.com/file/d/18sYdI0OOnh7_R54paY0wFEh1DuqrWmeo/view
Vacuna SINOPHARM®: características, esquema de vacunación, condiciones de conservación y uso, contraindicaciones, precauciones y efectos adversos más frecuentes.
En el presente documento también se puede acceder a la comparación entre las vacunas disponibles hasta la fecha para la Campaña de vacunación: Sputnik V®, COVISHIELD® y SINOPHARM®.
https://drive.google.com/file/d/12gqTrlB5xtvnT-Xkf1THCZrtQFcL1gNe/view
Fuente: Dirección de Control de Enfermedades Inmunoprevenibles (DiCEI), Ministerio de Salud de la Nación | Campaña Nacional de Vacunación contra la COVID-19 | Fecha: 18 de febrero 2021.
Manual del Vacunador Vacuna COVISHIELD
En el Manual se brindan las generalidades de la Campaña Nacional de Vacunación contra la COVID-19 y las especificaciones de la vacuna contra la COVID-19 COVISHIELD® (ChAdOx1nCoV-19 recombinante) que utiliza como plataforma un vector viral no replicativo (adenovirus de chimpancé).
Acceda al sitio oficial clicando sobre el siguiente enlace: https://bancos.salud.gob.ar/sites/default/files/2021-02/manual-vacunador-covishield.pdf
Fuente: Dirección de Control de Enfermedades Inmunoprevenibles (DiCEI), Ministerio de Salud de la Nación | Campaña Nacional de Vacunación contra la COVID-19 | Fecha: 10 de febrero 2021.
Manual del Vacunador Vacuna SPUTNIK V
Se incluyen las actualizaciones que se incorporan a los Lineamientos técnicos para la Campaña Nacional de Vacunación contra la COVID-19.
https://bancos.salud.gob.ar/sites/default/files/2021-02/actualizacion-manual-vacunador-sputnik-v-10-02-21.pdf
Informe de seguridad en vacunas. Vacunación COVID-19 en Argentina.
Fuente: DiCEI (Dirección de Control de Enfermedades Inmunoprevenibles) del Ministerio de Salud y Comisión Nacional de Seguridad en Vacunas.
Publicado 20 de enero de 2021.
Desde el inicio de la Campaña Nacional de Vacunación contra COVID-19 se han notificado, hasta las 18 hs del 14 de enero de 2021, al Sistema Integrado de Información Sanitaria de Argentina (SIISA) 8.841 ESAVI posteriores a la vacunación tras la aplicación de 195.490 dosis reportadas en el Registro Federal de Vacunación Nominalizado (NoMiVac) registradas hasta registradas hasta la fecha y hora señaladas.
Acceda al informe en : https://www.argentina.gob.ar/sites/default/files/4to-informe-seguridad-en-vacunas-20_01.pdf
Acompañamos este artículo con el link para reporte on line en el siguiente enlace donde se encuentra el instructivo de notificación a través de la plataforma SIISA: https://bancos.salud.gob.ar/recurso/instructivo-de-notificacion-de-esavi-online
Recuerde completar sus datos de contacto (telefónico y correo electrónico) para que el destinatario pueda asegurar una comunicación rápida ante eventos que requieran iniciar una investigación inmediata.
La notificación puede ser realizada por cualquier integrante del equipo de salud y debe realizarse dentro de las primeras 24 horas en los casos de ESAVI graves, y dentro de la primera semana en el resto de los eventos no graves.
Ampliación del informe técnico sobre la autorización de uso de VacunaGam-COVID-Vac (Sputnik V)
Fuente: Administración Nacional de Medicamentos, Alimentos y Tecnología Médica | ANMAT informa.
Publicado 20 de enero de 2021.
ANMAT recomendó incluir al grupo etario de mayores de 60 años.
Esta Administración Nacional comunica que, luego de analizada la nueva información aportada para la vacuna VacunaGam-COVID-Vac (Sputnik V), se estableció, por medio del informe de ampliación, que la misma se encuentra en un margen aceptable la seguridad, inmunogenicidad y eficacia para el grupo etario de mayores de 60 años.
En el análisis inicial sobre el perfil regulatorio de VacunaGam-COVID-Vac (Sputnik V) de diciembre de 2020, se mencionó que los datos de eficacia, inmunogenicidad y seguridad respecto a la población total del estudio con franja etaria 18 a 87 años reportaba un perfil de seguridad aceptable y que no hubieron eventos adversos inesperados hasta el momento del análisis.
Descargue el informe de ampliación (ANMAT, 20/01/2021) desde el enlace: https://www.argentina.gob.ar/sites/default/files/ampliacion_del_informe_tecnico_de_perfil_regulatorio_sobre_autorizacion_sputnik_v.pdf
Toda la información sobre la vacuna Sputnik V
Sitio del Centro Gamaleya destinado a las últimas noticias sobre la vacuna Sputnik V donde podrás encontrar información detallada y actualizada junto a preguntas frecuentes.
Sitio web: https://sputnikvaccine.com/
Lineamientos técnicos para la Campaña Nacional de Vacunación contra la COVID-19
Autor: Dirección de Control de Enfermedades Inmunoprevenibles
Año: 23/12/2020
Se presentan los lineamientos generales para el abordaje de la Campaña Nacional de Vacunación contra la COVID-19 la cual se encuentra bajo la dirección del Gobierno Nacional y se encuentra coordinada por el Ministerio de Salud Nacional, e incluye la participación y colaboración intersectorial de otras carteras del gobierno nacional, las 24 jurisdicciones y expertos de diversas áreas.
Esta campaña tiene como objetivo disminuir la morbilidad-mortalidad y el impacto socio-económico ocasionado por la COVID-19 en Argentina, a través de una campaña escalonada y progresiva con priorización en una primera instancia de personal de salud y riesgo.
Descarga la información en : https://bancos.salud.gob.ar/recurso/lineamientos-tecnicos-de-la-campana-de-vacunacion-contra-el-covid-19
El Ministerio de Salud de la Nación autorizó la vacuna SPUTNIK V
La ANMAT luego de recibir la información sobre la seguridad y eficacia de la vacuna del Instituto Gamaleya por la Comisión Nacional de Inmunizaciones ha prestado su conformidad para la autorización en época de pandemia de la vacuna Sputnik V.
Fuente: Ministerio de Salud de la Nación.
Publicado el miércoles 23 de diciembre de 2020.
Por resolución del ministro de Salud de la Nación, Ginés González García, se autoriza con carácter de emergencia la vacuna Gam-COVID-Vac, denominada Sputnik V, desarrollada por el Centro Nacional Gamaleya de Epidemiología y Microbiología de Rusia.
La autorización surge tras la visita de un equipo técnico de la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT) a las plantas donde se elaboran las vacunas y luego de acceder a la información sobre su seguridad y eficacia mayor al 91 por ciento, como así también a la que indica que no se han presentados eventos adversos graves, ni se han identificado diferencias significativas en la eficacia observada en los diferentes grupos etarios que participaron de los ensayos clínicos.
La vacuna Sputnik V está elaborada en base de una plataforma probada basada en vectores adenovirales humanos y requiere una segunda dosis luego de 21 días.
Acceda a más noticias sobre Sputnik V en el sitio oficial haciendo clic en
https://www.argentina.gob.ar/noticias/informe-de-la-anmat-sobre-la-vacuna-sputnik-v
Informe técnico https://www.argentina.gob.ar/sites/default/files/if-2020-89983542-apn-anmatms.pdf
Las vacunas de ARNm, una nueva forma de generar inmunidad contra SARS-CoV-2
Fuente: Rafael Sirera | Inmunoensayos.
Publicado: 17/12/2020.
“Conseguir una vacuna eficaz y rápida ante una pandemia por un virus emergente requiere dos puntos cruciales:
- En primer lugar, precisión y efectividad en el diseño de antígeno viral.
- Y en segundo lugar una plataforma de fabricación que sea capaz de acortar el tiempo de disponibilidad del producto en el mercado.
Las vacunas basadas en subunidades de proteínas y producidas en líneas celulares suelen tardar más de un año en generarse. Por el contrario, la fabricación de vacunas de ácido nucleico (ADN y ARN mensajero, ARNm) se puede lograr en cuestión de semanas.
La aprobación de una vacuna de ARNm para el coronavirus significa, por un lado, la autorización de la primera de su tipo contra enfermedades infecciosas. Y por otro lado una revolución en el concepto que teníamos hasta ahora de diseñar y elaborar vacunas.”
En este artículo podemos encontrar las diferentes vacunas según su elaboración (vector viral o ARN), su manera de acción, vacunas ARN y ADN, ventajas de las vacunas de ácidos nucleicos, descripción de la estructura del ARN mensajero, como es el mecanismo de su inmunogenicidad, Efectos secundarios y estabilidad y limitaciones de las vacunas de ARNm
Todo el desarrollo de esta información en: https://inmunoensayos.blogs.upv.es/2020/12/17/las-vacunas-de-arn-una-nueva-forma-de-generar-inmunidad-contra-sars-cov-2/
Respuesta del Ministerio de Salud de Córdoba sobre las Formulaciones Magistrales de Ibuprofenato de Sodio
Protocolo de Vacunacion PAMI
Informacion sobre Covid-19
 Aires Acondicionado y COVID 19
Aires Acondicionado y COVID 19
 Luces y sombras del tratamiento de Covid-19
Luces y sombras del tratamiento de Covid-19
 Situación epidemiológica Córdoba al 01 de octubre 2020 - Ministerio de Salud
Situación epidemiológica Córdoba al 01 de octubre 2020 - Ministerio de Salud
 Manejo seguro de Medicamentos, Productos Médicos y sanitarios en la Farmacia Hospitalaria
Manejo seguro de Medicamentos, Productos Médicos y sanitarios en la Farmacia Hospitalaria
 Protocolo de actuación desde la Farmacia Comunitaria
Protocolo de actuación desde la Farmacia Comunitaria
 Encuesta sobre el rol del farmacéutico: informe de resultados
Encuesta sobre el rol del farmacéutico: informe de resultados
 Dispositivos de protección respiratoria para personal de la salud - UNC
Dispositivos de protección respiratoria para personal de la salud - UNC
 Pronunciamiento CFC sobre el producto "Miracle Mineral Solution" (MMS)
Pronunciamiento CFC sobre el producto "Miracle Mineral Solution" (MMS)
 Protocolo de Bioseguridad - COE
Protocolo de Bioseguridad - COE
 Protocolo Control Sanitario Industrial
Protocolo Control Sanitario Industrial
 Mitos y verdades sobre Covid-19 - Informe Red CIMLAC
Mitos y verdades sobre Covid-19 - Informe Red CIMLAC
 Afiche consejos sobre Coronavirus
Afiche consejos sobre Coronavirus
 Medicamentos antihipertensivos e infección por COVID-19
Medicamentos antihipertensivos e infección por COVID-19
 23 preguntas y respuestas sobre Coronavirus
23 preguntas y respuestas sobre Coronavirus
 Lineamientos para farmacéuticos - FIP
Lineamientos para farmacéuticos - FIP
 Recomendaciones para equipos de salud - Ministerio de Salud de la Nación
Recomendaciones para equipos de salud - Ministerio de Salud de la Nación
 Resumen informativo 2019-nCoV - CFC
Resumen informativo 2019-nCoV - CFC
Vacunas Antigripales y Neumococcicas 2020
Informacion sobre DENGUE
 Resumen informativo | Dengue | Observatorio de Salud, Medicamentos y Ambiente CFC
Resumen informativo | Dengue | Observatorio de Salud, Medicamentos y Ambiente CFC
 Recomendaciones generales para el descarte de objetos
Recomendaciones generales para el descarte de objetos
 Guía para la participación social en la prevención del dengue
Guía para la participación social en la prevención del dengue
 PLANILLA DE DERIVACIÓN DE PACIENTES
PLANILLA DE DERIVACIÓN DE PACIENTES
Quinolonas y fluoroquinolonas de uso sistemico. Nuevas restricciones de uso por efectos adversos incapacitantes e irreversibles.
 Fluoroquinolonas - Informe CIME diciembre 2019
Fluoroquinolonas - Informe CIME diciembre 2019
Informe CIME sartanes (ARA II)
Estimados Farmacéuticos:
Este informe fue elaborado considerando la preocupación, por parte de pacientes y profesionales de la salud, debido a la presencia de impurezas en medicamentos pertenecientes al grupo de los antagonistas de los receptores de la angiotensina II ( ARA-II).
Alerta Epidemiologico sobre Rubiola
Estimado Farmacéutico
Ante las últimas noticias relacionadas con el caso importado de rubéola, que se presentó en la Provincia de Córdoba, enviamos link adjunto del Alerta Epidemiológico del Ministerio de Salud de la Nación, y adjuntamos las siguientes recomendaciones:
Prestar asesoramiento al paciente y recordarle que verifique y complete el esquema de vacunación de acuerdo a la edad, el cual debe acreditar:
-
De 12 meses a 4 años: UNA DOSIS de vacuna triple viral (sarampión-rubéola-paperas)
-
Mayores de 5 años: deben acreditar DOS DOSIS de vacuna con doble o triple viral después del primer año de vida
-
Las personas nacidas antes de 1965 no necesitan vacunarse porque son considerados inmunes
Se les solicita a todos los profesionales intensificar la vigilancia epidemiológica de casos sospechosos de enfermedad febril exantemática (EFE) y prestar especial atención a las mujeres en edad fértil que presenten contacto con casos sospechosos.
EL PRINCIPAL OBJETIVO DE EVITAR LA RUBÉOLA ES PREVENIR EL SÍNDROME DE RUBÉOLA CONGÉNITO.
Considerar como sospecho y de derivación urgente a todo paciente con fiebre (temperatura axilar mayor a 38ºC) y exantema, o cualquier caso en que el profesional de la salud sospeche sarampión o rubéola.
Recomendar mantener las medidas de higiene habituales para evitar contagios ( lavado frecuente de manos, no compartir utensilios con pacientes enfermos, utilizar pañuelos descartables, alcohol en gel, estornudar sobre el pliegue del codo, etc)
Ante cualquier duda comunicarse con nuestra Área de Capacitación y Responsabilidad Social, al T.E.: 0351-4249511 int 230-231-264 o vía mail a:formacion@colfacor.org.ar
Alerta_epidemiologica_RUBEOLA.pdf
Mag. Farm Maria Isabel Tenllado
Coordinadora
Área de Capacitación y Responsabilidad Social. CFC

